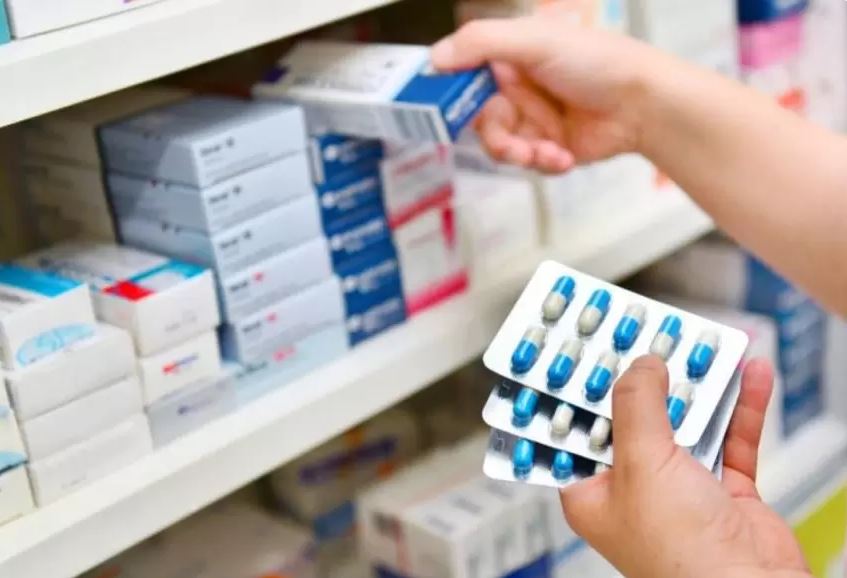
Berlín, 2 de febrero (EFE).- Los directores de los organismos de control y aprobación de medicamentos de Alemania, Austria y Suiza coincidieron este miércoles durante un congreso en Berlín en la necesidad de simplificar los trámites para acelerar el acceso al mercado de productos innovadores, algo que es posible según demostró la pandemia del covid-19.
«La innovación y la regulación no tienen que ser cosas opuestas», dijo el director del ente regulador suizo Swissmedic, Raimund Bruhin, durante el panel «Acceso al mercado de medicinas y terapias innovadoras» del congreso DACH Healthcare Innovation, organizado por Bamberg Health, compañía con la EFE mantiene un acuerdo de difusión para este contenido.
El director del ente alemán, BfArM, Karl Broich, por su parte, dijo que hay que estudiar qué procesos se pueden simplificar para acelerar la aprobación de medicamentos y vacunas y facilitar su acceso al mercado.
«A veces una de las razones que retrasan los procesos es que las empresas tardan en contestar nuestras preguntas. Pero nosotros también tenemos que preguntarnos si hacemos demasiadas preguntas o si no hacemos las preguntas correctas», dijo para añadir que durante la pandemia se mostró que es posible «acelerar procesos de autorización».
Bruhin y su homólogo austriaco Günter Waxenecker coincidieron en que los entes de control no se pueden limitar a esperar a que las empresas y los centros de estudios presenten solicitudes de aprobación para estudiarlas. «El proceso de aprobación no debe empezar con la presentación de una solicitud.
Tenemos que ser proactivos, trabajar con las empresas y los centros de estudios, estar al tanto de lo que están haciendo», dijo Bruhin.
«En Austria hemos abierto la posibilidad de que las empresas nos presenten sus proyectos», añadió Waxenecker. La tecnología puede ayudar, según añadió Broich, a que el uso de la digitalización y de la inteligencia artificial puedan simplificar trámites y señaló que la relación de su organismo ha cambiado con el tiempo.
«Cuando empecé a trabajar en BfArM nos veíamos como un organismo de protección del consumidor. Ahora la visión ha cambiado y entendemos que tiene que haber un intercambio con la industria», explicó.
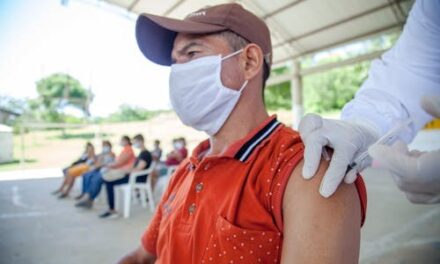
De parte de la industria, la directora de relaciones políticas del fabricante alemán de vacunas Novavax advirtió que para que las innovaciones lleguen a la gente no sólo se necesita su aprobación por parte de los organismos de control sino también que se les abra acceso al mercado.
En ese sentido se quejó, en la presentación «De la pandemia a la endemia: el futuro de la vacunación contra la covid-19», de que de todos los contratos de vacunas contra el covid-19 sólo uno ha sido renovado, lo que lleva a la creación de un monopolio y de una dependencia que puede poner en peligro el suministro.
Durante el evento el panel dedicado a las innovaciones en el sector de salud y la aceleración de los procedimientos para su acceso al mercado hubo otros, como el dedicado a la digitalización y el que abordaba las innovaciones administrativas en el sector sanitario.
El público al que se dirige el congreso son reguladores y funcionarios, representantes de ministerios de Salud y otras agencias gubernamentales involucradas en políticas y regulaciones de atención médica, así como emprendedores y empresas emergentes que trabajan en el campo de la tecnología y la innovación sanitaria y médicos, entre otros profesionales del sector. EFE